
Osteoartrosi, la terapia chirurgica alla luce delle nuove tecniche interventistiche
A cura di Alessandro Gildone
Casa di cura S. Maria Maddalena, Occhiobello (Rovigo)
Humanitas Medical Care (via Domodossola, 9A), Milano
Email: dottalessandrogildone@gmail.com
www.alessandrogildone.com
L’artrosi, o osteoartrosi, è una delle cause più frequenti di disabilità della popolazione adulta. Infatti, la sua prevalenza si assesta al 13,9% dei soggetti oltre i 25 anni di età, per poi colpire il 33,6% della popolazione sopra i 65 anni (1).
È inoltre la più frequente patologia articolare, considerato che si stima che colpisca in Europa circa 40 milioni di persone (2). Tuttavia non è semplice fornire numeri esatti sull’incidenza e la prevalenza di questa patologia, poiché non sempre si nota una correlazione tra sintomatologia clinica e segni radiografici.
Ma cosa si intende per artrosi? L’artrosi è una patologia eterogenea e, per maggior chiarezza, in questo articolo utilizzeremo la definizione data dall’OARSI (Società Internazionale per la Ricerca sull’Osteoartrosi) che così la definisce: “L’osteoartrosi è una patologia che interessa le articolazioni mobili, caratterizzata da stress cellulare e degradazione della matrice extracellulare causate da micro- e macro-lesioni che innescano maldestre risposte riparative. La patologia si manifesta dapprima con uno squilibrio molecolare (anormale metabolismo delle cellule dei tessuti articolari), seguito da uno squilibrio anatomico e/o fisiologico (caratterizzato da degradazione della cartilagine, rimodellamento osseo, formazione di osteofiti, infiammazione articolare e perdita della normale funzione articolare) che portano inevitabilmente alla comparsa della malattia” (3) (Figura 1).
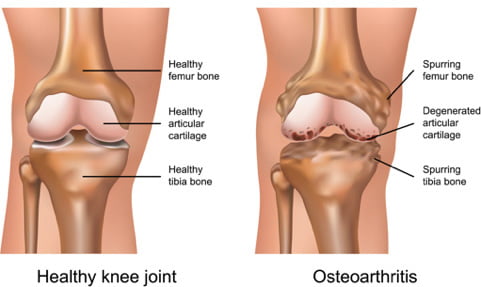
Da un punto di vista eziologico, l’osteoartrosi è una patologia complessa, con molteplici fattori di rischio, sia costituzionali (età, sesso femminile, obesità, familiarità) che meccanici (pregressi traumi articolari, sovraccarico funzionale causato da attività lavorative e/o sportive, malallineamento, lassità generalizzata) (4,5) (Figura 2). I primi causano la cosiddetta artrosi primitiva, i secondi l’artrosi secondaria.
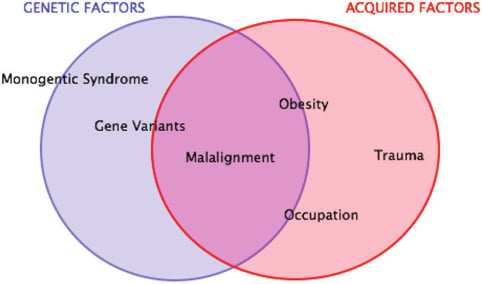
Da un punto di vista clinico la malattia si manifesta con dolore, limitazione del movimento, rigidità, crepitio e versamento articolare; da un punto di vista anatomopatologico si osserva fibrillazione, fissurazione o perdita a tutto spessore della cartilagine, formazione di osteofiti, ispessimento dell’osso subcondrale e infiammazione della membrana sinoviale.
L’osteoartrosi può virtualmente colpire qualsiasi articolazione, ma è nettamente più frequente nel ginocchio, nell’anca, nella colonna vertebrale e nella mano. Per gli scopi di questo articolo tratteremo in particolare le articolazioni del ginocchio e dell’anca.
Trattamento conservativo
Il principale obiettivo del trattamento dell’artrosi deve essere il controllo del dolore, con conseguente miglioramento della funzione articolare e della qualità della vita dei pazienti, cercando di evitare la potenziale tossicità dei farmaci; pertanto, in prima istanza, il trattamento si focalizza sugli esercizi fisioterapici e sui farmaci, ricorrendo all’opzione chirurgica in caso di fallimento del trattamento conservativo (6).
La gestione dell’artrosi è passata dall’approccio tradizionale di controllo del dolore all’adozione di misure che potessero migliorare la funzione articolare e la qualità della vita. Pertanto, il miglior approccio conservativo dell’artrosi deve includere un approccio sia farmacologico che non, che fermi il cronico avanzare della malattia (7).
La terapia non farmacologica consiste nell’associazione di esercizi fisioterapici, controllo del peso corporeo, esercizi di rinforzo muscolare e utilizzo di tutori (8). Alcune metanalisi hanno dimostrato che l’esercizio fisico garantisce risultati simili a quelli ottenuti con i FANS in termini di sollievo dal dolore e miglioramento della funzione (9); in questo senso si consigliano esercizi volti al rinforzo muscolare, allo stretching e alla flessibilità, meglio se eseguiti in acqua (10). Recenti studi hanno anche dimostrato come un efficace programma fisioterapico possa ridurre l’utilizzo del paracetamolo nei pazienti affetti da osteoartrosi dell’anca e del ginocchio (11).
Anche l’utilizzo di stampelle, tutori di ginocchio e plantari può aiutare a ridurre il dolore e migliorare la funzione dell’articolazione (12-14).
Per finire, altrettanto importante è il discorso del controllo del peso corporeo. Un recente trial clinico, infatti, ha dimostrato un miglioramento del 50% della sintomatologia nei pazienti che erano stati in grado di ridurre il proprio peso corporeo del 10% con la dieta e l’esercizio fisico (15).
Per quanto riguarda l’approccio farmacologico, i FANS sono spesso ritenuti i farmaci di prima scelta, poiché hanno mostrato un’efficacia simile o superiore al paracetamolo (16,17). Tuttavia gli effetti dannosi dovuti all’assunzione cronica dei FANS sono ben noti, in particolare sull’apparato gastrointestinale, renale e cardiovascolare, causando più di 16.500 morti e ricoveri ospedalieri all’anno solo negli USA (18). Questi effetti dannosi interessano sia i FANS tradizionali che i COX-2 selettivi, anche se questi ultimi sembrano essere più sicuri e tollerati.
La durata ottimale della terapia con FANS non è chiara; una metanalisi di studi clinici randomizzati (19) non ha evidenziato una chiara correlazione tra la durata della terapia con FANS e il rischio di eventi cardiovascolari. Un altro trial cinico ha sottolineato una miglior efficacia sul dolore con l’utilizzo continuo del celecoxib piuttosto che al bisogno, con rischio simile di eventi avversi (20).
A causa degli eventi avversi causati dai FANS, si è sempre considerato il paracetamolo come farmaco di scelta nel trattamento del dolore lieve o moderato causato dall’artrosi. In realtà, le recenti linee guida sul trattamento dell’artrosi ne sconsigliano l’utilizzo come farmaco di prima scelta (8,21); infatti, uno studio randomizzato controllato ha dimostrato come il paracetamolo al dosaggio di 4 g al giorno avesse gli stessi effetti del placebo sul dolore causato dall’artrosi del ginocchio (22). Inoltre, altri studi clinici hanno messo in evidenza come il paracetamolo possa causare effetti dannosi alla salute, in particolare in pazienti con comorbidità (23).
Le infiltrazioni intrarticolari con cortisone riducono il dolore per un breve periodo di tempo (1-2 settimane in studi clinici randomizzati) e migliorano la funzionalità articolare nei pazienti affetti da artrosi. Si possono prendere in considerazione nei pazienti che si presentano con dolore acuto e versamento articolare; tuttavia, è sconsigliato ricorrere al cortisone intrarticolare per più di una volta ogni 4 mesi, considerato che questo farmaco può danneggiare il tessuto cartilagineo (24,25) e aumentare il rischio di infezioni.
Anche l’acido ialuronico è un farmaco ampiamente utilizzato nelle infiltrazioni intrarticolari, ma i benefici non sono chiari secondo alcune metanalisi; alcuni studi riferiscono solo un lieve beneficio sul dolore (26), mentre altri riportano un sollievo sul dolore più duraturo rispetto al cortisone, superiore alle 8 settimane (27).
Gli oppiacei rappresentano un’alternativa per quei pazienti che non riescono a tollerare i farmaci di prima scelta a causa della presenza di comorbidità. Le revisioni sistematiche hanno concluso che gli oppiacei per os o per via transdermica sono più efficaci rispetto al placebo nel trattamento del dolore da artrosi dell’anca e del ginocchio. Tuttavia, i benefici sono risultati molto limitati, mentre gli effetti collaterali hanno costretto molti pazienti ad abbandonare il trattamento; inoltre, l’utilità degli oppiacei nel lungo periodo pare essere limitata (28) e la loro somministrazione si associa a un rischio maggiore di eventi avversi rispetto ai FANS, tra cui le fratture, le patologie cardiovascolari e la mortalità in generale (29).
Nel vasto ambito dei trattamenti alternativi, l’utilizzo degli integratori alimentari gioca un ruolo sempre più importante; tra questi la glucosamina è senza dubbio quello maggiormente utilizzato. Tuttavia, studi clinici randomizzati hanno evidenziato come il suo effetto sul dolore sia paragonabile a quello del placebo (30). Così come per la glucosamina, anche nei confronti della condroitina i lavori sono scettici nell’attribuirle un ruolo sul dolore artrosico; alcuni studi infatti hanno mostrato qualche beneficio nell’utilizzo della condroitina, mentre altri no (31,32). Anche la sua capacità di modificare il decorso della malattia appare dubbio; alcuni lavori, infatti, hanno evidenziato rispetto al placebo un rallentamento della riduzione dello spazio articolare, soprattutto se in associazione con la glucosamina (33), ma se usata da sola le differenze non si sono rivelate statisticamente significative (34).
Per finire alcuni cenni su terapie più recenti, quali le cellule mesenchimali, opportunamente prelevate e trattate; allo stato attuale non ci sono evidenze scientifiche a supporto del loro utilizzo. In particolare, la Società Internazionale per la Ricerca delle Cellule Staminali e l’Associazione Australiana dei Reumatologi ne sconsigliano vivamente l’uso routinario nell’osteoartrosi.
Trattamento chirurgico
In caso di grave degenerazione articolare, ribelle al trattamento conservativo, bisogna ricorrere all’intervento di sostituzione protesica dell’articolazione. Le procedure artroscopiche, infatti, non garantiscono al paziente risultati migliori rispetto alla fisioterapia e al trattamento farmacologico (35,36).
● Le nuove tecniche mininvasive
La sostituzione protesica di un’articolazione affetta da artrosi rappresenta sempre l’ultima opzione, da considerare in caso di fallimento delle altre terapie precedentemente descritte. Nonostante l’elevato grado di invasività di questa procedura chirurgica, i risultati sono sempre stati molto buoni, sia da un punto di vista del recupero funzionale che del miglioramento della sintomatologia dolorosa e della qualità di vita (37). Inoltre, il miglioramento dei design protesici e dell’usura del polietilene (l’inserto in plastica che permette il movimento della protesi) garantiscono una longevità sempre maggiore degli impianti.
Tuttavia, è risaputo che una minore aggressività nei confronti dei tessuti molli quali cute e muscoli permette una migliore guarigione della ferita oltre a una più rapida riabilitazione articolare; la sfida, però, è ridurre il trauma chirurgico ai tessuti mantenendo tuttavia la visibilità del sito chirurgico necessaria per effettuare l’intervento.
Un intervento mininvasivo, pertanto, viene definito come una procedura che sia sicura e che riesca nel contempo a minimizzare il trauma chirurgico dei tessuti molli rispetto a una procedura cosiddetta convenzionale. I vantaggi di tale approccio si traducono in un ridotto dolore postoperatorio, in una più breve degenza ospedaliera e in un più rapido recupero funzionale. Solitamente una minore invasività dell’atto chirurgico si associa a una minore incisione cutanea: tuttavia, se questa è ovviamente una prerogativa imprescindibile, piccola incisione chirurgica non necessariamente sta a significare intervento mininvasivo, perché anche i tessuti sottocutanei andranno rispettati il più possibile, al fine di migliorare la guarigione del paziente. Il concetto di mininvasività, pertanto, si ispira a una filosofia di risparmio dei tessuti in modo che il paziente possa recuperare più rapidamente (38), e non si focalizza semplicemente sulla lunghezza dell’incisione chirurgica. In un’ideale tecnica chirurgica mininvasiva, quindi, i tessuti sottocutanei vengono risparmiati il più possibile, divaricati e non incisi, fino ad arrivare al piano chirurgico interessato, perché il rispetto dei tessuti molli correla con una migliore funzionalità articolare e con un più rapido recupero (39).
Nella ricerca della migliore via chirurgica, pertanto, si sono indirizzate le tecniche mininvasive, sia per quanto riguarda la protesica di ginocchio che, soprattutto, quella dell’anca.
Per quanto riguarda la protesica di ginocchio, i primi lavori relativi alla mininvasività risalgono alla fine degli anni ‘90, quando alcuni chirurghi iniziarono a consigliare l’utilizzo di protesi monocompartimentali (Figura 3) per trattare l’artrosi di una parte del ginocchio (40).
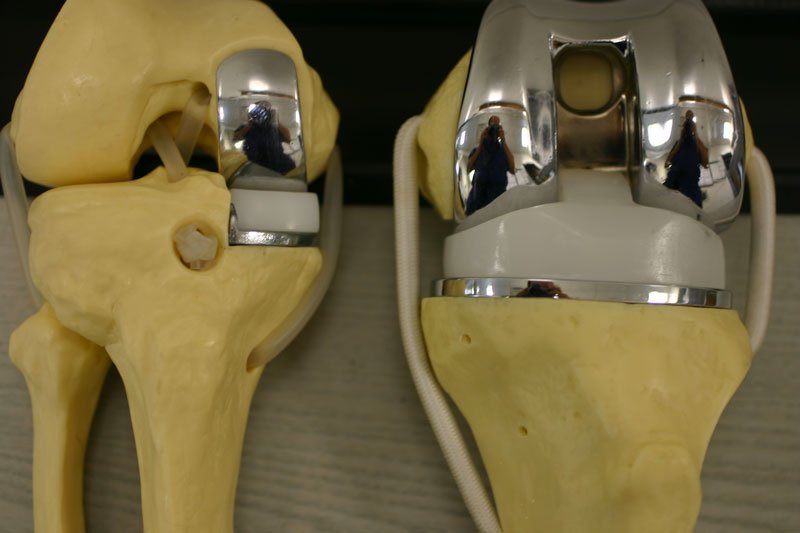
Perché sostituire tutta l’articolazione del ginocchio se solo una parte è danneggiata dall’artrosi?
Il concetto di mininvasività inteso come rispetto dei tessuti nell’eseguire il medesimo intervento, tuttavia, ha iniziato a svilupparsi all’inizio degli anni Duemila, sulla scorta delle esperienze accumulate in precedenza nel campo della protesica di anca. I primi lavori dimostrarono come ridurre l’incisione chirurgica e rispettare il più possibile le strutture sottocutanee diminuissero le perdite ematiche e il dolore postoperatorio, migliorando nel contempo la riabilitazione con conseguente riduzione dell’ospedalizzazione e dei tempi di recupero (41). Ma come applicare i concetti di mininvasività alla protesizzazione del ginocchio? I primi sforzi si sono diretti verso una via di accesso chirurgica sempre migliore, che risparmiasse per esempio il tendine quadricipitale, il motore dell’estensione del ginocchio normalmente inciso durante gli approcci convenzionali (Figura 4).
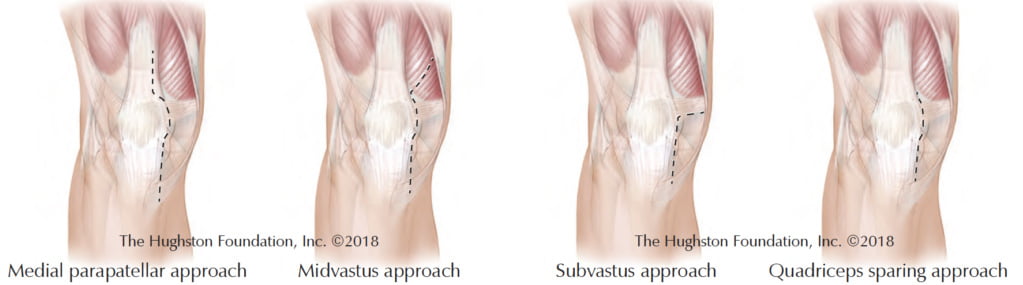
La riduzione dell’incisione chirurgica, tuttavia, ha reso subito evidente come lo strumentario utilizzato fosse del tutto inadeguato alla mininvasività in termini di grandezza e di ingombro dello spazio, rendendo necessaria la progettazione di nuova strumentazione e nuovi design protesici, che potessero facilitare la procedura chirurgica mininvasiva (42,43).
La stessa filosofia della mininvasività si applica anche alla protesizzazione dell’anca, un intervento che ha dato grosse soddisfazioni per più di 40 anni in termini di riduzione del dolore e miglioramento della funzionalità.
Anche in questo campo, infatti, si è sempre pensato che un grande intervento come la protesi d’anca potesse essere eseguito solo con grandi incisioni chirurgiche; tuttavia, il concetto di “grande chirurgia-grande incisione” è stato messo decisamente in discussione negli ultimi 10 anni, proprio nel tentativo di limitare i danni iatrogeni dei tessuti. A questo proposito, per quanto riguarda la chirurgia protesica dell’anca, gli accessi chirurgici mininvasivi si dividono in due gruppi: da un lato quelli che riducono l’incisione chirurgica e dei tessuti muscolari (accesso laterale e posteriore), dall’altro quelli che arrivano all’articolazione dell’anca cercando di risparmiare i gruppi muscolari evitandone del tutto l’incisione tramite una, due o più mini-incisioni cutanee, quali l’accesso anteriore (Figura 5).
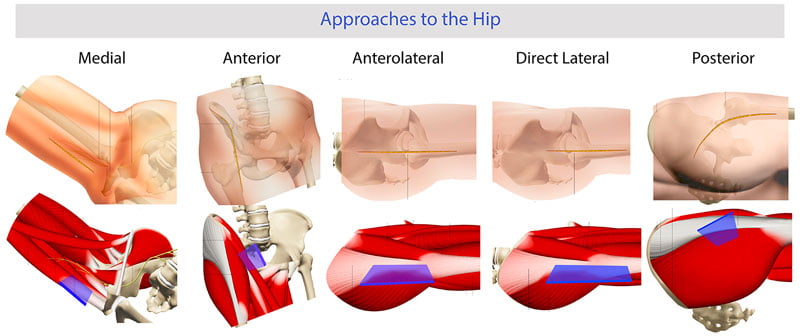
Ancor più che nella protesica di ginocchio, la ricerca di vie di accesso chirurgiche all’anca sempre più piccole e meno traumatiche ha richiesto la modificazione degli strumentari chirurgici necessari all’impianto di una protesi, che nel tempo sono diventati sempre più piccoli e, soprattutto, “offsettati”, cioè non su un unico asse ma su assi differenti, al fine di poterli introdurre nel campo operatorio con maggiore facilità.
Le tecniche mininvasive per la protesica articolare, tuttavia, anche se molto attraenti sia per il chirurgo che per il paziente, devono essere in grado di rispettare i principi cardine per un risultato ottimale: il posizionamento dell’impianto, l’allineamento, la fissazione della protesi all’osso e il rispetto della normale biomeccanica articolare sono caratteristiche imprescindibili per il risultato a lungo termine dell’impianto protesico.
Considerato che il concetto di mininvasività si associa anche a una riduzione dell’incisione e quindi del campo chirurgico, talvolta risulta difficile visualizzare alla perfezione le strutture che andremo a trattare. Ed è proprio nell’ottica di poter aiutare il chirurgo a gestire strutture non perfettamente visualizzabili che si sono sviluppate di recente nuove tecniche assistite dal computer, che permettono la navigazione computerizzata di siti anatomici non (o mal) visualizzabili direttamente.
● La chirurgia ortopedica assistita dal computer
Per chirurgia ortopedica assistita dal computer (CAOS) si intende un particolare tipo di chirurgia che si avvale di tecnologie che partecipano direttamente all’atto chirurgico o di sistemi che intervengono attivamente nell’atto chirurgico, ma che possono aiutare il chirurgo nel posizionamento navigato nello spazio degli strumenti chirurgici (44). In particolare, la CAOS include sommariamente tre sistemi, ognuno con importanti, ma distinte funzioni: sistemi passivi, sistemi semi-attivi e sistemi attivi.
I sistemi passivi non sono in grado di eseguire alcun gesto chirurgico sul paziente, ma giocano un ruolo fondamentale nell’aiutare il chirurgo a pianificare preoperatoriamente l’intervento e a fargli posizionare correttamente l’impianto durante l’intervento. La navigazione nello spazio è la loro principale caratteristica; un esempio è Optotrack 3020, un sistema che sfrutta la luce a infrarossi per fornire informazioni durante l’intervento.
A differenza dei sistemi passivi, i sistemi semi-attivi eseguono alcune azioni quali muovere un trapano o una sega grazie a un braccio robotico; tuttavia, questi sistemi non eseguono tali azioni autonomamente, ma necessitano sempre dell’azione diretta del chirurgo (es. Acrobot o Mako). Per finire, i sistemi attivi eseguono atti chirurgici programmati prima dell’intervento; un esempio di sistema attivo è ROBODOC, che prepara autonomamente il canale femorale per il posizionamento protesico sulla scorta di informazioni che gli sono state assegnate dal chirurgo sulla base del piano preoperatorio (Figura 6).

In linea di massima, tutti i sistemi CAOS seguono 4 passaggi: l’impostazione, la registrazione, la pianificazione e l’esecuzione. La formazione del modello virtuale del sito anatomico può sfruttare indagini strumentali preoperatorie (TAC o RMN), oppure basarsi sui dati acquisiti durante l’intervento, a seconda del sistema utilizzato (Figura 7).
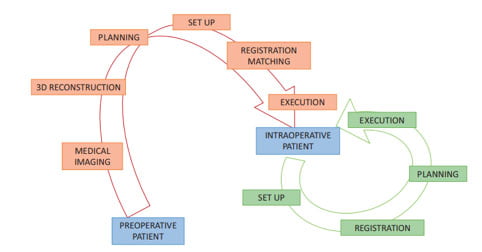
Per impostazione si intende il posizionamento dei dispositivi atti a rilevare le strutture di nostro interesse e a posizionarle nello spazio: si fissano saldamente delle antenne nell’osso del paziente e si posizionano in sala operatoria i dispositivi che parteciperanno all’intervento (per es. videocamere e/o robot). Per registrazione si intende l’ottenimento delle coordinate dei vari punti nello spazio, in modo da ricreare sul computer un modello virtuale del sito anatomico da operare. Tutti e tre i diversi sistemi visti in precedenza utilizzano tecnologie differenti per la registrazione: indagini strumentali preoperatorie, quali la TAC e la RMN (es. MAKO), indagini strumentali intraoperatorie come la fluoroscopia, soprattutto nella chirurgia spinale e traumatologica, acquisizione intraoperatoria dei dati senza ausilio di indagini strumentali. Per pianificazione si intende lo scopo vero e proprio dell’intervento in oggetto: sul modello virtuale presente nel computer si posizionano le componenti protesiche a seconda del desiderio del chirurgo. Il processo termina con l’esecuzione dell’atto chirurgico: il computer guida il chirurgo nell’esecuzione dei tagli ossei sulla base della pianificazione eseguita (Figura 8). Il chirurgo, tuttavia, non è obbligato a seguire le indicazioni del computer, ma può in qualsiasi momento modificare il piano chirurgico.
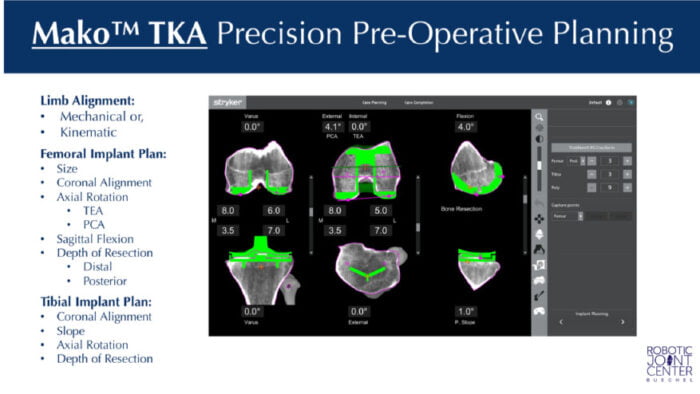
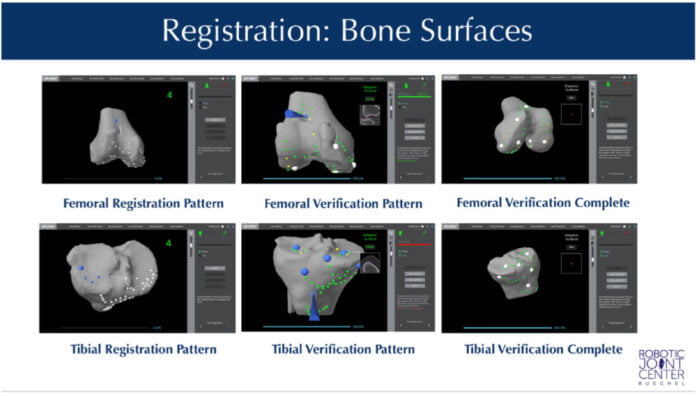
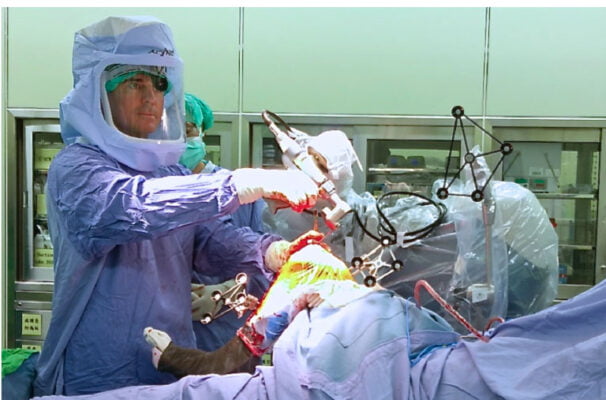
Qualunque sia il sistema utilizzato, pare evidente come il processo della registrazione dei dati sia quello più importante, attraverso il quale passa tutto il sistema della chirurgia assistita dal computer. L’accuratezza e la precisione rappresentano il focus della chirurgia assistita dal computer, che ha come obiettivo quello di ridurre i possibili errori umani allo scopo di migliorare i risultati clinici; la qualità della registrazione, pertanto, gioca un ruolo fondamentale per ottenere un atto chirurgico estremamente preciso, necessario per garantire la longevità dell’impianto protesico (45).
Nell’intervento di protesizzazione dell’anca, per esempio, un allineamento corretto dell’impianto migliora la funzionalità e la durata dell’impianto protesico (46). In particolare, il fattore che più preoccupa il chirurgo è il posizionamento nello spazio della componente acetabolare che, se mal posizionata, potrebbe causare impingement, ridotta escursione articolare e aumentato rischio di lussazioni (47).
L’introduzione della chirurgia assistita dal computer ha ridotto il rischio di malposizionamento della componente acetabolare, rendendo l’atto chirurgico accurato e facilmente riproducibile (48). Un’altra caratteristica di questo tipo di chirurgia è la capacità di misurare la lunghezza degli arti e di consentire con maggiore facilità le tecniche minivasive (49); queste tecniche, infatti, per definizione limitano il campo visivo del chirurgo che, quindi, necessita della navigazione fornita dal computer per poter posizionare al meglio le componenti protesiche. Come già detto, la navigazione assistita permette anche di essere più accurati nella misurazione della lunghezza degli arti dopo inserimento della protesi d’anca; le dismetrie degli arti inferiori, infatti, sono causa di rigidità, dolore e di fallimento dell’impianto, oltre a rappresentare la principale causa di insoddisfazione e di rivalsa legale da parte del paziente (49,50).
Anche nell’ambito della protesica di ginocchio la chirurgia assistita dal computer gioca un ruolo fondamentale. Infatti, per poter garantire un buon risultato, il chirurgo deve essere in grado di dare all’impianto protesico e all’arto il miglior allineamento possibile (51). Un allineamento appropriato, infatti, permette al ginocchio di essere stabile e mobile, caratteristiche fondamentali per una buona qualità di vita.
La chirurgia assistita dal computer permette di standardizzare l’allineamento dell’arto, riducendo le variabili dovute all’errore umano. Inoltre, l’utilizzo del computer ha permesso di abbandonare le guide intramidollari, che si è visto essere responsabili di un rischio aumentato di embolia polmonare gassosa, una delle complicanze più frequenti durante la protesizzazione del ginocchio (52).
D’altro canto però, l’utilizzo di complessi dispositivi tecnologici allunga la durata dell’intervento chirurgico, senza ridurre l’incidenza di infezioni o eventi tromboembolici (53) e richiede una curva di apprendimento più lunga da parte del chirurgo.
Considerazioni conclusive
In definitiva, la chirurgia assistita dal computer ha rivoluzionato lo scenario della moderna chirurgia ortopedica, ma il suo utilizzo non è né universale né perfetto poiché, come detto, oltre agli innegabili vantaggi esistono alcuni svantaggi, tra cui l’elevato costo e il fatto che la letteratura scientifica non è concorde nell’affermare con certezza che le modificazioni date dalla chirurgia assistita dal computer si traducano poi in un effettivo miglioramento clinico. Tuttavia è anche vero che la navigazione con il computer permette al chirurgo una migliore visibilità del sito chirurgico, offrendo la possibilità di affidarsi con maggior sicurezza alle tecniche mininvasive.
Bibliografia
1. Lawrence RC et al. Estimates of the prevalence of arthritis and other rheumatic conditions in the United States. Part II. Arthritis Rheum. 2008; 58(1): 26–35. 2. Bannwarth B, Kostine M. Targeting nerve growth factor (NGF) for pain management: what does the future hold for NGF antagonists? Drugs 2014; 74(6): 619-26. 3. Kraus VB et al. Call for standardized definitions of osteoarthritis and risk stratification for clinical trials and clinical use. Osteoarthritis Cartilage 2015; 23(8): 1233-41. 4. Radin EL et al. Relationship between lower limb dynamics and knee joint pain. J Orthop Res 1991; 9: 398–405. 5. Radin EL et al. Animal joint behavior under excessive loading. Nature 1970; 226: 554–555. 6. Gamble R et al. Recommendations for the medical management of osteoarthritis of the hip and knee. Arthritis and Rheumatism 2000; 43(9): 1905–1915. 7. Hunter DJ. Lower extremity osteoarthritis management needs a paradigm shift. Br J Sports Med 2011; 45: 283-8. 8. McAlindon TE et al. OARSI guidelines for the non-surgical management of knee osteoarthritis. Osteoarthritis Cartilage 2014; 22: 363-88. 9. Zhang W et al. OARSI recommendations for the management of hip and knee osteoarthritis: Part III: Changes in evidence following systematic cumulative update of research published through January 2009. Osteoarthritis Cartilage 2010; 18: 476-99. 10. Fransen M, McConnell S. Land-based exercise for osteoarthritis of the knee: a metaanalysis of randomized controlled trials. J Rheumatol 2009; 36: 1109-17. 11. van Baar ME et al. The effectiveness of exercise therapy in patients with osteoarthritis of the hip or knee: a randomized clinical trial. Journal of Rheumatology 1998; 25(12): 2432–2439. 12. Jones A et al. Impact of cane use on pain, function, general health and energy expenditure during gait in patients with knee osteoarthritis: a randomised controlled trial. Ann Rheum Dis 2012; 71: 172-9. 13. Raja K, Dewan N. Efficacy of knee braces and foot orthoses in conservative management of knee osteoarthritis: a systematic review. Am J Phys Med Rehabil 2011; 90: 247-62. 14. van Raaij TM et al. Medial knee osteoarthritis treated by insoles or braces: a randomized trial. Clin Orthop Relat Res 2010; 468: 1926-32. 15. Messier SP et al. Effects of intensive diet and exercise on knee joint loads, inflammation, and clinical outcomes among overweight and obese adults with knee osteoarthritis: the IDEA randomized clinical trial. JAMA 2013; 310: 1263-73. 16. Pincus T et al. A randomized, double-blind, crossover clinical trial of diclofenac plus misoprostol versus acetaminophen in patients with osteoarthritis of the hip or knee. Arthritis Rheum 2001; 44: 1587-98. 17. Pincus T et al. Preference for nonsteroidal anti-inflammatory drugs versus acetaminophen and concomitant use of both types of drugs in patients with osteoarthritis. J Rheumatol 2000; 27: 1020-7. 18. Wolfe MM et al. Gastrointestinal toxicity of nonsteroidal antiinflammatory drugs. N Engl J Med 1999; 340: 1888-9. 19. Chou R et al. Analgesics for osteoarthritis: an update of the 2006 comparative effectiveness review. Comparative Effectiveness Reviews, No. 38. Report No. 11-eHC076-EF. Rockville (MD): Agency for Healthcare Research and Quality (US); 2011 20. Luyten FP et al. A prospective randomised multicentre study comparing continuous and intermittent treatment with celecoxib in patients with osteoarthritis of the knee or hip. Ann Rheum Dis 2007; 66: 99–106. 21. Bannuru RR et al. Reassessing the role of acetaminophen in osteoarthritis: systematic review and meta-analysis. Osteoarthritis Cartilage 2010; 18 Suppl 2: S250. 22. Miceli-Richard C et al. Paracetamol in osteoarthritis of the knee. Ann Rheum Dis 2004 ;63: 923-30. 23. Craig DG et al. Staggered overdose pattern and delay to hospital presentation are associated with adverse outcomes following paracetamol-induced hepatotoxicity. Br J Clin Pharmacol 2012; 73: 285-94. 24. Hochberg MC et al. Guidelines for the medical management of osteoarthritis. Part II. Osteoarthritis of the knee. American College of Rheumatology. Arthritis Rheum 1995; 38: 1541-633. 25. Raynauld JP et al. Safety and efficacy of long-term intraarticular steroid injections in osteoarthritis of the knee: a randomized, double-blind, placebo-controlled trial. Arthritis Rheum 2003; 48: 370-7. 26. Rutjes AW et al. Viscosupplementation for osteoarthritis of the knee: a systematic review and meta-analysis. Ann Intern Med 2012; 157: 180-91. 27. Bannuru RR et al. Therapeutic trajectory of hyaluronic acid versus corticosteroids in the treatment of knee osteoarthritis: a systematic review and meta-analysis. Arthritis Rheum 2009; 61: 1704-11. 28. Nüesch E et al. Oral or trans-dermal opioids for osteoarthritis of the knee or hip. Cochrane Database Syst Rev 2009: CD003115. 29. Solomon DH et al. The comparative safety of analgesics in older adults with arthritis. Arch Intern Med 2010; 170: 1968-76. 30. Clegg DO et al. Glucosamine, chondroitin sulfate, and the two in combination for painful knee osteoarthritis. N Engl J Med 2006; 354: 795-808. 31. Reichenbach S et al. Meta-analysis: chondroitin for osteoarthritis of the knee or hip. Ann Intern Med 2007; 146: 580-90. 32. Hochberg MC. Structure-modifying effects of chondroitin sulfate in knee osteoarthritis: an updated meta-analysis of randomized placebo-controlled trials of 2-year duration. Osteoarthritis Cartilage 2010; 18 Suppl 1: S28-31. 33. Hochberg MC et al. The rate of decline of joint space width in patients with osteoarthritis of the knee: a systematic review and meta-analysis of randomized placebo-controlled trials of chondroitin sulfate. Curr Med Res Opin 2008; 24: 3029-35. 34. Fransen M et al. Glucosamine and chondroitin for knee osteoarthritis: a double-blind randomized placebo-controlled clinical trial evaluating single and combination regimens. Ann Rheum Dis 2015; 74: 851-8. 35. Kirkley A et al. A randomised trial of arthroscopic surgery for osteoarthritis of the knee. N Engl J Med 2008; 359: 1097-107. 36. Katz JN et al. Surgery versus physical therapy for a meniscal tear and osteoarthritis. N Engl J Med 2013; 368: 1675-84. 37. Neuprez A et al. Total joint replacement improves pain, functional quality of life, and health utilities inpatients with late-stage knee and hip osteoarthritis for up to 5 years. Clin Rheumatol 2020; 39: 861-71. 38. Ljungqvist O et al. Enhanced recovery after surgery: a review. JAMA Surg 2017; 152(3): 292–298. 39. Lonner JH. Minimally invasive approaches to TKA: results. Am J Orthop 2006; (Belle Mead NJ); 35(7 Suppl): 27–29. 40. Repicci JA, Eberle RW. Minimally invasive surgical tech-nique for unicondylar knee arthroplasty. J South Orthop Assoc 1999; 8(1): 20–27. 41. Haas SB et al. Minimally invasive total knee replacement through a mini midvastus approach: a comparative study. Clin Orthop Relat Res 2004; 428: 68–73. 42. Tria AJ Jr. Minimally invasive total knee arthroplasty: the importance of instrumentation. Orthop Clin North Am 2004; 35(2): 227–234. 43. Bonutti PM et al. Minimally invasive total knee arthroplasty. J Bone Joint Surg 2004; 86-A(suppl 2): 26–32. 44. Jenny JY. The history and development of computer assisted orthopaedic surgery. Orthopade 2006; 35: 1038–1042. 45. Cartiaux O et al. Accuracy of computer-aided techniques in orthopaedic surgery: how can it be defined, measured experimentally, and analyzed from a clinical perspective? J Bone Joint Surg Am 2017; 99: e39. doi:10.2106/JBJS.15.01347. 46. Sikorski JM, Chauhan S. Computer- assisted orthopaedic surgery: do we need CAOS? J Bone Joint Surg Br 2003; 85: 319–323. 47 Jolles BM et al. Computer-assisted cup placement techniques in total hip arthroplasty improve accuracy of placement. Clin Orthop Relat Res 2004; 426: 174–179. 48. Taylor RH. Computer–Integrated Surgery: Technology and Clinical Applications. Cambridge: MIT, 1996. 49. Kelley TC, Swank ML. Role of navigation in total hip arthroplasty. J Bone Joint Surg Am 2009; 91 (Suppl. 1): 153–8. 50. Parvizi J et al. Surgical treatment of limb-length discrepancy following total hip arthroplasty. J Bone Joint Surg Am 2003; 85: 2310–17. 51. Wasielewski RC et al. Wear patterns on retrieved polyethylene tibial inserts and their relationship to technical considerations during total knee arthroplasty. Clin Orthop Relat Res 1994; 229: 31–43. 52. O’Connor MI et al. Fat emboli in total knee arthroplasty: a prospective randomized study of computer-assisted navigation vs standard surgical technique. J Arthroplasty 2010; 25: 1034–40. 53. Bauwens K et al. Navigated total knee replacement. A meta–analysis. J Bone Joint Surg Am 2007; 89: 261–269.


